1차 시험 단어장
- atomic force microscopy {cantilever}
- optical tweezers
- micro pipette aspiration (microaspiration)
- Traction force microscopy
- analytical ultra centrifuge
- dynamic light scattering
- multi angle light scattering
- size exclusion column\
- mass spectrometry {}
- Tandom mass spectrometry
partial molar volume
partial specific volume
sedimentation coefficient
stokes radius
1st week
고저니
질량과 주기와 용수철상수의 관계를 문제로 내신다고 한대요
locomotion(걸어가기)
왜 진자의 주기는 진자 길이에만 영향을 받는가? 질량과 진폭에는 상관이 없고?
F는 각가속도에 질량과 진자 길이를 곱한 량으로 이어진다. 왜냐면 이게 선가속도니까.
그래서 각에 대한 미분방정식은
작은 각에 대한 근사
이건 조화 진동자이다. 각진동수가
이렇게 되는. 주기를 구하면
이렇게 된다.
왜 질량의 영향이 없어지는가?
질량이 클 수록 관성이 커지지만, 중력에 의해 받는 힘 또한 커지기 때문.
시험 대비
조화진동자
진동수는 용수철 상수와 질량으로 주어진다.
당연히 용수철 상수가 셀 수록 진동수가 높아지고, 질량이 커질 수록 진동수가 낮아지겠지?
진동수와 각진동수의 관계는?
진동수: 단위 시간에 얼마나 ‘돌았느냐’
각진동수: 단위 시간에 얼마나 ‘각도가 바뀌었느냐’
그래서 각진동수는 진동수보다
주기는 진동수의 역수. 주기를 T라고 한다면
2nd week
motion을 이용한 실험
질문: 분자나 세포에게서 어떤 움직임을 볼 수 있을까?
질문: 분자나 세포에 영향을 주는 요소는? ECM, inter-cellular interaction, cell motion, intra-cellular metworks
왜 이런 질문이 필요한가?
모델은 시스템과 factor에 의해 결정된다.
대표적인 예시 cell migration(wound healing) 이런 예시는 고전적인 힘에 지배된다.
이 운동에 대한 단순한 모델이 있다고 한다. 좋은 모델은 모든 parameter를 다루는 모델이 아니라 관찰 내용을 잘 설명하는 모델이다.
세포의 속도와, 세포의 수(질량)
문제가 생기는 경우: 케라틴 네트워크를 못 만들고 응집되는 경우, 세포가 움직이고 고정될 기판이 없다. 피부가 찰흙같이 된다. 이 상태에서는 앞서 wound healing과 다른 모델로 세포가 움직인다. 오히려 세포 이동 속도가 느리다고 한다. 유체에 의한 저항을 받는다.신호도 안 간다. 때문에 재생이 안 된다. 이 사례는 케라틴의 존재 여부로 인해 유효한 모델이 완전 바뀜을 보인다.
모델은 시스템에 달려있다.
flagella or cillia등 motor system에 의한 운동. 이 꼬리들이 회전 운동을 하는지, 좌우 운동을 하는 지에 따라 모델이 바뀐다.
cillia는 한번에 여러 개의 형태를 찍을 수 있으니까, 시간에 따른 모양 변화를 관찰하기 쉽다.
이 운동 기관에서 비롯된 힘 정도는 알 수 있다.
살펴볼 실험
- atomic force microscopy {cantilever}
- optical tweezers
- tools for cell mechanics (dynamics)
- micro pipette aspiration (microaspiration)
- Traction force microscopy
- analytical ultra centrifuge
- dynamic light scattering
- MALS
- size exclusion column
Atomic force microscopy
표면을 긁는 탐침(cantilever, 스프링같음)이 표면과 상호작용하는 힘을 이용해 이미징. 상호작용에는 인력과 척력 모두가 작용한다. 원자 사이 상호작용하고 똑같다. 너무 가까이에 있으면 척력이 작용하며, 적당히 멀리 떨어져 있으면 인력이 작용한다.
세포 표면 볼 수 있다. 이미징하니까 세포가 울퉁불퉁하다. 단백질 분자도 볼 수 있다.
탐침이 샘플과 접촉하는 방법에 따라 세 가지 모드로 분류한다.
- contact mode, 이것에는 노이즈가 낄 수 있다. 벽에 걸릴 때마다 탐침이 팅팅 튀기 때문이다. 그래서 아래 두 가지 방법을 사용한다.
- non-contact mode, 탐침을 샘플에서 약간 떨어진 거리에 둔다. 울퉁불퉁한 표면에 의해 거리가 살딱 가까워질 때, 인력으로 탐침이 휜다.
- tapping mode, 탐침을 샘플에 붙였다 뗐다가 한다.
이들의 이미지 차이는 오렌지색 이미지가 있는 슬라이드에서 확인할 수 있다.
→ 자료가 날라갔어!
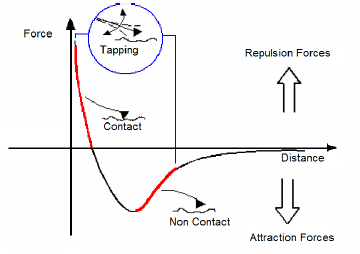
반데르발스힘, 원자의 인력과 척력, 적당한 거리에서 힘을 측정하는 것이 중요하다.
구성요소 네 가지
cantilever, laser, quadrant photo detector, sample stage
탐침에 레이저를 쏘아서, 탐침이 흔들리는 정도를 측정한다. 반사된 위치가 멀 수록(탐침의 위치와 레이저 디텍터의 위치가 멀 수록) 작은 각도 변화도 크게 측정될 수 있다.
뉴턴 역학과 cantilever의 훅의 법칙
훅의 법칙을 이용해 cantilever가 휘어진 각도를 알면 당시의 힘이 뭔지 간단하게 알 수 있다.
s가 탐침이 평형지점에서 벗어난 거리, k가 탐침의 용수철 상수라면,
k를 사전에 알고 s를 측정했으니 F를 알 수 있다.
single molecule mechanics에서 응용
이러면 이미징도 가능하지만 분자 사이의 힘을 알 수도 있다.
탐침에 상호작용하는 분자를 단다면? 분자 사이 인력을 측정할 수 있다.
예시 실험 1
DNA양쪽 가닥의 상호작용하는 힘은 어떨까?
두 가닥이 붙을 때와 떨어질 때의 힘은 어떨까?
한 탐침에 4base의 서열을 달고, 시료에는 상보적인 서열을 달아둔다.
나노 뉴턴 단위 힘도 측정할 수 있다고 한다. 진짜 수소 결합 수준의 힘이다.
예시 실험 2
세포에서 측정되는 힘의 지도를 만들어보자. 세포가 단단한 곳을 찾는다.
아니면 세포 자체의 단단함을 측정할 수도 있다.
세포가 핵 주변에서 단단함을 실제로 측정할 수 있었다. (핵막 단백질은 튼튼했다)
나머지 부분은 물처럼 말랑했다.
어떤 세포는 세포 골격이 단단하여 그것 또한 느낄 수 있었다.
세포의 단단한 정도를 측정해서 암세포와 정상 세포를 구별하는 시도가 있었다.
특히 전이가 잘 되는 암과 아닌 암을 구별했다.
malign은 더 말랑했고 benign은 더 단단했다.
예시 실험 3
핵막의 NPC(nuclear pore complex)를 측정한다. 이것은 핵막의 물질 유출입을 관리하는 문지기역할을 한다. 이게 진짜 직경에 변화가 있는지를 AFM으로 관찰했다.
NPC뿐만 아니라, 주변의 핵막 단백질 lamin또한 변형됨을 알 수 있었다.
피코뉴턴 수준의 힘이 주어지면 변형 가능한다. 큰 것이 유출입하려면 큰 힘을 주어 포어를 벌릴 수 있다는 것을 알 수 있었다.
NPC는 유동적인 친구였구나!
optical tweezers
이것도 힘 측정하는 도구다. 그런데 이건 레이저 자체가 힘을 준다.
레이저 안 쪽에 있는 반투명 비드는 일부 빛을 투과시켜서 힘을 받는다.
들어오는 빛의 운동량과 나가는 빛의 운동량의 차이가 비드로 전해진다.
즉, 빛이 굴절되는 방향으로 광자에 힘이 주어진다.
반작용으로 비드는 레이저의 안쪽으로 끌려가게 된다.
이 벡터 그림은 꼭 그려라! 시험에 나온다.
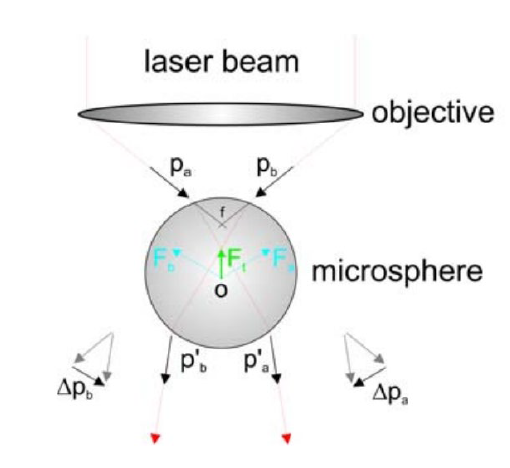
빛의 세기와 파장, 둘 다 힘의 계산에 영향을 준다.
비드에 레이저를 쏘아서, 비드를 띄워서, 비드에 물체를 달아서, 당기고 할 수 있다.
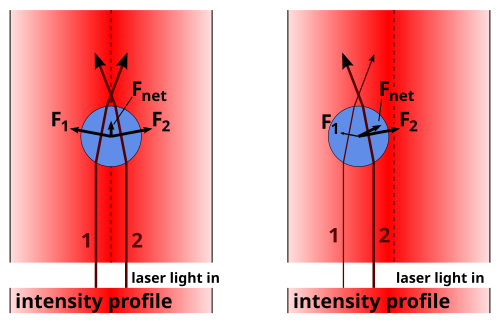
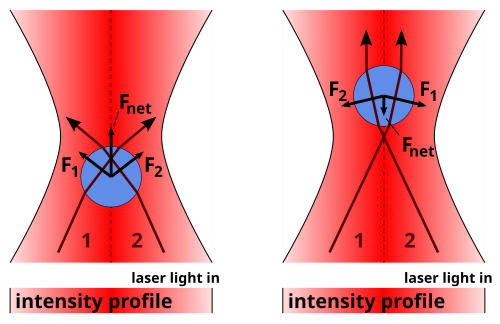
빛을 가우시안으로 쏘기 때문에, 비드는 빔의 가운데로 향하려고 한다. harmonic potential과 같이 작용한다고 한다. 비드에 가해지는 외부 힘을 비드의 위치를 이용해 알 수 있게 된다.
예시 실험 1
단백질을 당겨서 접힘 풀림의 힘을 측정하기
RNase H에 대한 실험. 잘 접히고 잘 풀리는 단백질로 유명하다.
이 접힘 풀림 또한 pN 단위이다.
이전 까지는 단백질의 힘을 열역학적 에너지로만 계산했는데,
이제는 힘을 직접 측정할 수 있게 되었다.
Cell mechanics
말 그대로 세포의 힘을 다루는 연구 주제.
누르거나, 인력을 측정하거나.
이 연구 주제를 연 것은 AFM이다.
위에서 본 실험 말고, 다른 소박한 방법으로도 힘을 측정할 수 있다.
particle tracking microrheology → 세포 내부 물질의 확산 운동을 분석해서 내부에 있는 장애물의 분포를 확인한다.
magnetic probes → 작은 자석 탐침을 이용한다. 탐침의 운동을 확인한다.
micropipete aspiration → 마이크로 피펫을 찝어 빨아본다. 잘 빨리는지 확인해서 단단함을 측정한다.
microplate rheometer → 세포를 양쪽 판에 붙여서 당겨본다.
세포가 직접 움직일 때 바닥을 당기는 힘을 측정하자!
Traction force microscopy
아래 판에 스프링이 달린 형광을 달아놓고, 이게 당겨지는 정도를 측정하자.
세포가 당기는 판의 각 위치에서 힘을 구할 수 있다.
세포 힘의 지도를 알아서, 세포 각각의 스트레스를 구할 수 있다.
발제: 생체 분자의 질량을 어떻게 구하지?
왜 분자의 질량을 알아야 할까?
질량은 분자의 정체를 알아낼 때 좋은 단서가 될 수 있다.
전기영동은 문자의 무게와 크기를 대충 알 수 있는 방법이다. 그러나 해상도가 그리 높지 않은 한계가 있다.
질량 변화를 측정하면 생체 내 화학 반응을 추적하는 데 유용하다.
어떤 단백질이 서로 붙어 있는가? 어떤 단백질이 complex를 이루었나? 볼 수 있다는 뜻이다.
translation trascription은 모두 질량을 증거로 알아낸 결과라고 한다.
질량을 측정하려면 뭘 측정해야 하나?
힘과 가속도를 잘 측정해야 한다.
진동 운동. 질량에 따라 진동수가 바뀐다.
석영을 이용한다. 석영에는 위에 있는 질량과 전기에 의해 진동수가 바뀌기 때문이다.
quartz crystal microbalance
물질을 붙인 후, 진동수가 이전과 똑같아지는 전기를 측정한다.
mass spectrometry
이온을 붙이고, 힘을 주어서, 운동 궤적이 어떻게 변화하는지 보자.
이것을 통해 알 수 있는 것은 질량과 전하의 비율이다.
전하는 알고 있으니까, 질량을 알게 되는 것이다.
전하는 전기장에서 힘을 작을 것이다.
자기장을 받으면 이동 방향에 수직으로 힘을 받을 것이다.
자기장 구간에서 휘어서 이동한 반경을 이용해 힘을 알 수 있는 것이다.
자기장 구간에서 속도는 알고 있다.
속도를 이전 전기장 구간에서 준 전기에너지이기 때문이다.
전기장 구간에서 비행 시간을 측정하는 방법으로 TOF(time of flight)라고 한다.
이것의 정확도를 높이는 것은 긴 시간을 비행하게 두는 것이다.
이러기 위해 반복 달리기를 시킨다.
어떻게 입자를 정확한 전하를 가지게 만드는가? 이게 노벨상을 받았다.
MALDI (matrix assisted laser desorption ionization)
electrospray ionization
Tandom mass spectrometry
MS에 대한 자세한 소개
로렌츠 힘
힘은 전하와 속도와 자기장의 벡터곱.
원운동이 제일 기술하기 쉬움.
1테슬라는 10^4 가우스
테슬라 단위는 어마어마한 단위다.
원운동하는 전하에 대해 , 로렌츠 힘과 원심력의 등식을 세워라
그래서 질량분석기에서는 질량/전하 가 중요한 요소이다.
전기장을 가해서 원하는 속도로 만든다.
아는 속도로 날라간 전하가 자기장 영역에서 도는 원운동의 반지름을 구한다.
v와 B를 알고 있고 q도 알고 있으므로 m을 알 수 있다.
진공 유지가 중요.
질량분석기의 세 부분
ion source(MALDI, ESI) / mass analyzer(TOF, Quadrupole, Ion Trap, Orbitrap) / detector
MALDI
설명이 부실해
ESI(ElectroSpray)
이온화된 용액을 뿌린다? 어떻게?
Quadrupole
긴 -대전 막대 두 개와 + 대전 막대 2개.
x축과 y축을 관장하는 두 쌍의 막대
한 쌍은 직류로, 한 쌍은 교류로.
특정 m/z만 가진 이온만 통과할 수 있다.
특정 m/z가 아닌 경우, x나 y에 대해 위치 값이 발산하여 튕겨 나간다.
Ion trap
특정 이온 값만 선택해서 고이게 한다.
Fourier transform-ion cyclotron resonance
MS의 응용, 이용 방법
Tandem MS(MS/MS, 질량 분석 두 번 하기, 단백질을 두 번 쪼개서) = proteomics, post translational modification
HDX-MS =
Tandem MS
첫번째 단계에서 원하는 m/z만 모은다.
두 번쨰 단계에서 한번 더 단백질을 쪼개서 다시 찍는다.
m/z peak를 하나 골라서, 그 시료를 다시 쪼개서 다시 찍는다.
proteomics란?
한 세포, 조직, 기관 전체의 단백질 상태를 연구하는 것
세포에서 단백직 뽑는다. 효소(트립신으)로 단백질 대충 자른다. 씻는다. MS돌린다.
어떤 효소를 사용하는지에 따라 어디가 얼마나 잘릴 지 알 수 있다.
아미노산 서열에서 중간이 잘려서 생긴 작은 조각 이온을 daughter ion이라고 부른다.
그런데 잘리는 게 꼭 펩타이드 본드 부분이리라는 보장이 없다.
원래의 n 터미널이 있던 부분이 b(n)-ion, 나머지 부분이 y(m-n)-ion이다.
m은 전체 아미노산 수, n은 m이하의 자연수
모든 예상되는 b-ion과 y-ion이 나온다면 정말 예상한 ion이 맞는 것이다.
어떤 단백질을 MS 돌리면 peak가 어떻게 뜰지 프로그램으로 분석할 수 있다.
post translational modification
modification이 되어 있다면 그것이 포함된 peak의 위치가 달라진다.
HDX-MAX
N에 붙어있는 H는 자꾸 바뀐다.
hydrogen exchange(HX)
단백질이 있던 solvent를 중수소(D)로 바꾸면 어떨까?
질량이 달라진다! 그러면 어디에서 HDX가 일어나는지 알 수 있다.
아미노산과 시퀀스마다 HX가 일어나는 확률이 달라진다.
단백질 바깥에 교환 부위가 노출되어 있을 경우 높은 확률로 HX가 일어난다.
이 교환 부위가 노출되는 확률을 계산할 수 있다.
이건 NMR로 측정할 수도 있다.
MS로 찍으면 HX 여부에 따라 두 가지 peak가 있고, incubation 시간에 따라 양측 peak의 높이가 달라진다.
binding 여부를 연구할 수도 있다. binding 되면 교환 부위가 노출되지 않으므로
낮은 pH를 이용해 연구해야 하므로, 펩신밖에 사용할 수 없다.
시간에 따라 pH를 달리 하여 어디가 먼저 folding되는지 관찰할 수도 있다.
시험 문제
b-ion과 y-ion 을 주어주고 MS를 그려라. z값도 고려해서.
질량분석기를 위한 조건.
3rd week
유체의 흐름으로 파악하는 생명현상의 이해
지난 시간 까지는 생체분자의 무게를 측정했다.
분자량을 이용해서 단백질을 파악할 수 있다.
ms를 이용하지 않고 분자량을 측정하는 방법?
세포 내에서 큰 덩어리의 크기를 보는 방법? → 유체가 필요하다.
제일 쉬운 방법: 겔을 내린다. 크로마토그래피로 분리한다.
SDS page의 아쉬운 점 → 단백질의 조립이 풀린다
NATIVE page → 단백질 분해제를 없앰. 단백질이 조립된 상태 그대로 내려온다.
더 정확하게 측정하는 방법?→ 원심분리기, 광산란 특정법, 크로마토그래피
광산란법과 크로마토그래피를 같이 쓰면 원심분리기 만큼의 신용을 얻을 수 있다.
analytical ultra-centrifuge(AUC)
AUC는 돌리는 것과 해석이 어렵다.
fixed angle vs swing bucket → swing bucket이 분석에 유리하겠지.
원심력 공식
그런데 진공이 아니라 유체 속이다.
유체에 의한 저항이 작용. 저항은 속도와 선형적 비례
마찰끌림힘 공식
저항력과 원심력의 평형 상태를 이용해 m을 구하자.
질량을 알 수 있으면 생명 현상의 변화를 추적하는 게 쉬움
sedimentation coefficient, Svedberg unit (S)
s = v / (ω²r)
분모는 회전에 의한 가속도를 의미
분모 값이 거의 고정이라면, 침강 속도에 의해 s가 결정.
s다 클 수록 빠르게 침강한다.
그리고 질량이 클 수록 당연히 빠르게 침강한다. 강한 원심력을 받으니까
이것의 단위는 100펨토 세컨, 1S = 100fs
펨토는 10
침잠하는 데에 얼마나 시간이 걸리냐는 뜻.
한 분자가 10^7 m/s^2 의 가속도를 주었을 때(중력가속도 100배) 1초에 16um를 가면 그 입자는 16S이다.
S가 커질 수록 같은 시간에 더 멀리 간다는 것.
부분몰부피(partial molar volume), 구조에 따라서 물에 녹았을 때 부피 차이가 달라진다.
1은 용매, 2는 용질, n은 몰수, V는 혼합물의 부피
그러니까 부분 몰 부피는 각 성분 분자의 몰 양이 혼합물의 부피에 끼치는 영향이다 이말이야.
용매의 분자가 용질 분자에 딱 붙어서 잘 둘러 싸면, 혼합물의 부피 변화가 그리 크지 않을 것이고, 부분 몰 부피는 작아진다.
반면 용매와 용질의 상호작용이 약하다면 (이상 용액) 부분 몰 부피는 고정이며, 원래 물질 각각의 1몰당 부피와 동일할 것이다.
용매와 용질의 몰수가 아니라 질량을 아는 경우에는?
부분견줌부피(partial specific volume)을 이용한다.
g는 각 성분의 질량(그램 단위, 어째서!!)
이 과정에서
똑같은 양의 부피를 변화시키는 성분의 질량을 성분의 몰 수로 나눈 것이다.
두 개념을 이용해 정확한 혼합물의 밀도를 알 수 있다.
부력이 있을 때 분자의 겉보기 질량, 즉 부력 질량은 뭘까?
입자가 차지하는 공간에서
이때
밀도 기울기를 만들어 센트리를 돌리자. 큐브 안에 농도가 다른 탑을 만드는 것이다. 분자가 자신의 부력 질량이 0이 되는 곳에 도달하면, 그곳에서 더이상 원심력을 받지 못 하므로 멈춘다.
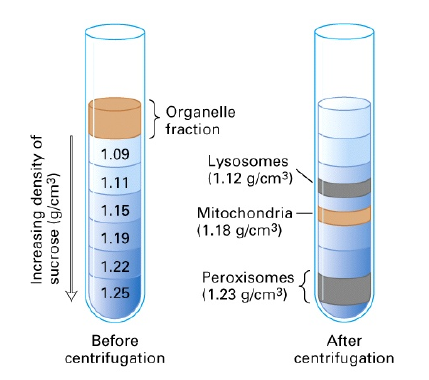
partial specific mass
유체 속의 질량은 부력이 반영된 것이다.
부력에 의한 효과는 partial specific volume과 solvent density의 곱이다.
solvent density도 다 알 수 있는 방법이 있다.
질량을 알아내는 두 가지 방법, 침전평형법과 침전속도법
침전평형법(sedimentation equilibrium)
용액 내 분자 밀도 기울기를 측정. (어떤 높이에 밀도가 얼마인지)
볼츠만 분포 이용.
두 위치에서 입자를 발견할 확률은 포텐셜 에너지 차이를 볼츠만 분포에 넣은 것.
위치에 따른 농도가 더이상 바뀌지 않는, 평형 상태에 다다랐을 때 농도 기울기를 이용해서 m’을 알 수 있다. partial specific volume은 예상 값으로 넣어 계산한다.. 아마도.
침전속도법(sedimentation velocity)
힘이 평형일 때 속도는 일정, 이 식을 통해 질량을 알 수 있다.
마찰계수는 용매의 점성과 모양(stokes radius)을 이용해서 알 수 있다.
이때 f는 마찰계수이다.
마찰 계수를 구하는 여러 방법
sedimentation coefficient를 생각해보자.
이건 시간에 불변이라고 가정하는 것 같다.
즉, 속도 분석을 통해 sedimentation coefficient를 알 수 있으며,
D를 알아 마찰계수를 알고 있다고 가정하면 m’를 구할 수 있다.
식을 살짝 변형해 보면,
m’를 안다면 혼합물의 밀도와 partial specific volume을 이용해 진짜 m을 구할 수 있다.
속도가 거리마다 변하므로, 적분을 이용해야 s를 정확히 구할 수 있다.
초기 위치와 시간이

왜 풀이식에서 상용로그를 쓰나요?
dynamic light scattering (DLS)
입자가 확산을 잘 하면, 확산 계수 D가 높아지면 입자가 활발히 움직일 것이다.
D에 관한 식으로 수정하면
dynamic light scattering은 빛을 이용해 D를 알아내고, 나머지 이미 아는 값을 이용해 R_s를 알아내며, 단백질이 대강 구형이라는 가정 하에 질량을 대충 구하는 방법이다.
흡광도를 측정하는 게 아니라, 산란된 빛들의 깜박임을(speckles, blinks) 측정한다.
입자가 많을 수록 산란이 맣이 된다.
입자가 열적으로 활발히 움직이면 산란광의 깜빡임이 심해진다.
입자의 열적 유동은 확산 계수로 주어진다.
입자가 브라운 운동하는 스텝 간격을 빛의 파장과 맞춘다.
빛이 산란되는 비율은 입자의 크기에 의해 결정.
입자가 크면 천천히 움직이고, 입자가 작으면 빠르게 움직인다.
움직이는 속도에 의해 산란광의 깜박임 속도가 달라진다.
세포와 단백질 수준은 판별 가능, 센서가 속도를 따라잡을 수 있다. (마이크로~미리 세크 단위)
물리학자들은 입력 신호들의 correlation time을 계산한다.
빨리 움직이면 correlation time이 짧겠지?
하나의 분자는 exponential decay하는 auto correlation function을 가진다.
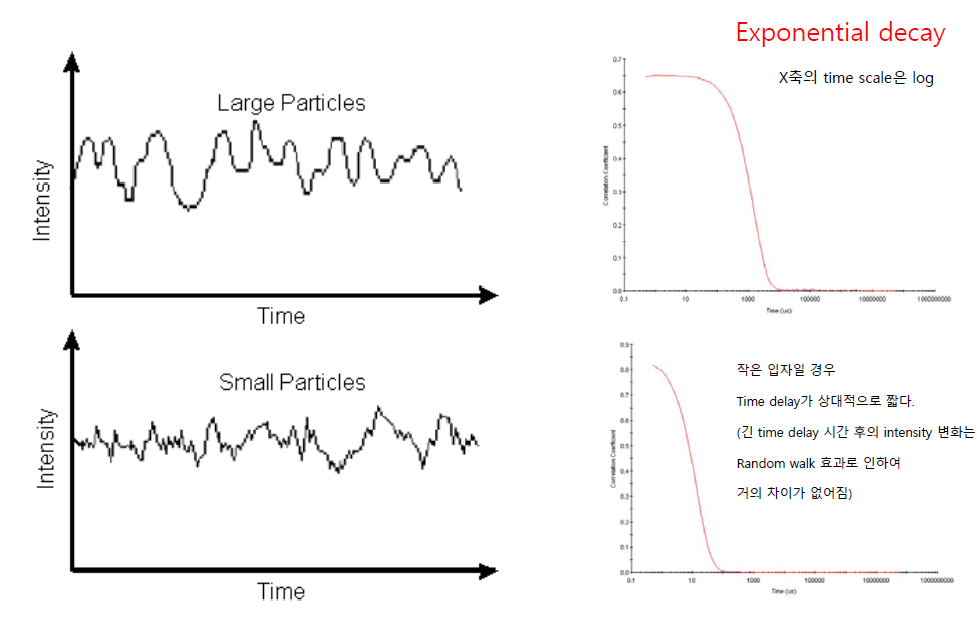
시간에 대한 auto correlation function을 분석하면, phase가 몇 개가 섞여있는지 알 수 있다. 다른 입자는 서로 다른 phase를 가지고 있다.
진동수가 선형적으로 결합되었기 때문.
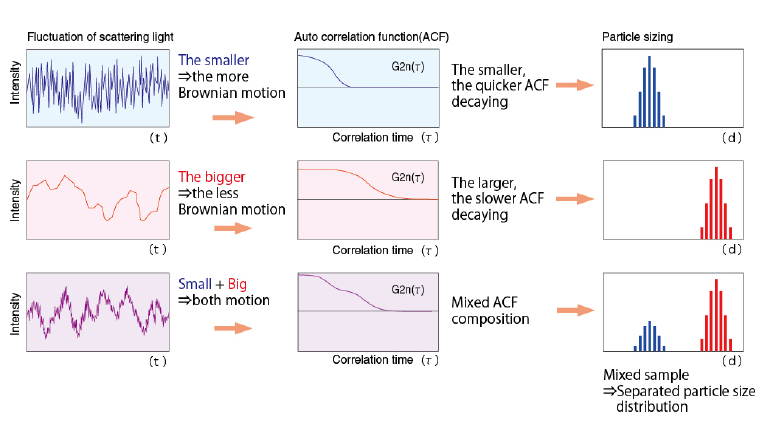
즉, DLS는 입자의 크기 분포를 측정할 수 있다.
대상이 구형 단백질이라면 밀도를 이용해서 분자량을 역산할 수 있다.
장) 빠르고 간편(20분~30분), 빠르고 실시간으로 변화를 관찰할 수 있음.
단) 기계가 비싸다
multi angle light scattering - MALS
레일리 산란과 미에 산란
빛의 파장과 편광
단파장의 편광된 빛을 쏘아서 다각도에서 산란광을 측정하자.
MALS는 레이리 산란 정도의 작은 입자를 취급한다. 이 산란은 각도에 따른 반응이 대칭적이다.
입자의 크기를 알 수 있다면 산란 각도에 따른 세기를 계산할 수 있다.
크기는 분자가 물에 녹아 생기는 밀도가 일정한 덩어리.
radius of gyration(
MALS를 이용하면 DLS와 다르게 분자의 크기와 분자가 구형에서 벗어난 정도를 알 수 있다.
반응은 농도와 각도에 대해 선형적이다.
이때 보이는 공간의 기울기는 입자가 원형에서 벗어난 정도를 나타낸다.
농도를 달리 하며 측정한다.
장) 정확, 분자량, 모양(R_g, 구형에서 얼마나 벗어났는지), 다 알려줌
단) 더럽게 비싸다. 시간이 살짝 더 걸린다. 샘플 하나에 하루 잡아먹음. 다 시간 많이 잡아먹는거, AUC가 낫지 않을까.
size exclusion chromatography (SEC)
porous bead를 고정상으로 이용.
크기가 작은 입자는 비드에 갇혀서 느리게 나오고, 크기가 큰 입자는 잘 통과해서 빠르게 나온다.
실험 조건만 맞추면 물질이 통과해 나오는 시간은 항상 똑같다.
원래는 이온을 없애고 단백질만 추출하는 desalting 과정에 쓰였다.
나오는 시간(흐른 용액 부피의 비율)이 분자량의 log값과 비례한다.
펌프가 일정하게 밀어주므로 속도는 일정.
물질이 나올 때까지 걸리는 부피는 입자기 여행한 경로의 길이와 선형적으로 비례힌다.
Ve/Vo
장) 싸다!! 재현성 좋다!!
단) 시간이 오래 걸린다. 내리는 데에는 시간이 얼마 안 걸리는데 비드 준비하는 데에 시간이 많이 걸린다. 하루종일! 그래서 평형상태의 분자량만 특정 가능. 다이나믹하게 바뀌는 걸 관찰할 수는 없음.
mass photometry - iSCAMS
interferomence scattering
따끈따끈하게 만들어진 장비
산란광의 크기를 측정한다.
입자가 작을 수록 그림자가 희미하고
입자가 클 수록 그림자가 진해진다.
역산란광을 사진 찍어서 확인하는 것이다.
특정 질량을 가진 입자지
레이놀드 넘버! 기억 안 난다. 공부한다!
유체역학
시험에 나올 것
질량 보존: 연속 방정식
에너지 보존: 베르누이 방정식
운동량 보존: 나비에 스토크스 방정식
레이놀드 넘버:
양자생물학
시험 안 나온다.
고전에서도 양자화가 일어날 수 있다. boundary condition이 있을 때, 정상파.