2차 시험 단어장
Levinthal’s paradox
Anfinsen’s dogma(이름에 n이 세 번 들어가는 구만)
differential scanning calorimetry(DSC) → 직접 측정하는 것은?
비열과 엔트로피, 온도의 관계식은?
isothermal tiltration calorimetry(ITC)
엔트로피 주도 반응과 엔탈피 주도 반응의 메카니즘 차이는?
microscale electrophoresis(MST)
differential scanning fluorimetry
equilibrium dialysis
surface plasmon resonance(SPR)
biolayer interferometry(BLI)
quartz crystal microbalance(QCM)
Foster resonance energy transfer(FRET)
electromyogram(EMG)
trans-epithelial electrical resistance(TEER)
electro encephalo graphy
magneto encephalo graphy
superconducting quantum interference device(SQUID)
SDS PAGE
CLARITY
iontophoresis
electrospary ionization
r: stokes radius
electrophoresis mobility:
detailed balance → 핵심 식을 설명하라.
Glauber dynamics
Matropolice dynamics
2차 시험 이창훈 교수님 열역학(ligand binding affinity)
지금까지는 입자 크기 측정법을 배웠다.
이제는 열역학적 성질을 알기 위한 열적 측정 방치를 배운다.
calorimetry
과학파트의 장비와 이번 주 배우는 장비를 비교해보라.
생명체의 열을 츨정했던 역사적인 실험
단열 용기 안에 생명체를.
얼음을 채워넣는다. 녹은 물의 양을 측정한다.
현대에도 비슷하다.
열을 잘 단열하고 온도를 측정한다.
열을 측정해서 뭘 할 것인가?
단백질의 folding unfloding에 필요한 열은 뭘까?
단백질에 리간드가 결합하는 데에 필요한 에너지는 얼마일까?
물질의 비열이 얼마일까? (잘 녹나 안 녹나?)
반응 전후의 깁스자유에너지 차이를 보면 반응 평형 상수를 볼 수 있다.
이거 Boltzman factor에 의한 transition rate와 똑같다!
에너지 단위가 1몰당이기 때문에 볼츠만 상수가 아닌 이상기체 상수를 사용한 듯 하다.
주로 invitro로 실험한다.
- 발열흡열을 측정
- 용액실험
- real-time 빠르게 볼 수 있고 변화를 볼 수 있어요. → dynamics, kinetics 측정 가능
- 분자 종류에 영향을 받지 않음
- 광학적 라벨링 필요없음 → 시간 많이 걸리는 작업을 안 해도 된다! 축복이여.
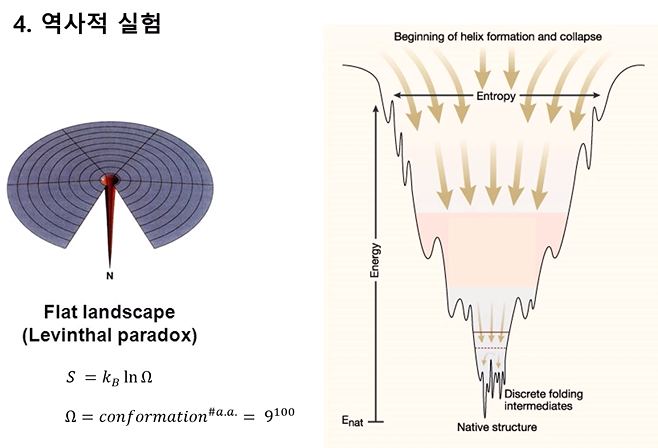
Levinthal’s paradox
사고실험
100개의 아미노산은 99+99개의 각도의 자유도를 가짐.
각 하나당 3개의 상태중 하나일 수 있다고 가정.
3^198 이면 얼마냐…10^94 정도의 숫자다.
컴퓨터로는 평생 계산 못해. 우주가 죽을때까지 못해.
이렇게 오래 걸리는 계산을 자연은 어떻게 하는 거지?
실제 가능한 구조의 경우의 수는 한정되어 있을 것이다.
자연의 접힘 과정은 어떤 규칙이 있을 것이다.
우리도 그 규칙을 찾아서 계산하자.
RNA분해효소(Ribonuclease A)는 정말 튼튼하다.
이거를 약물(Chaotropic reagent, urea 등) 치고 열 쳐서 기능을 불활성화 시켰는데, 방해요소를 없애니까 다시 기능이 살아난다. → 다시 접히는구나! 접힘은 가역적이구나!
Anfinsen’s dogma
단백질의 native한 접힘은 오로지 그것의 아미노산 서열에 의해 결정된다.
열적인 단백질 접힘
-
- 유일성 (Uniqueness) - 해당 서열이 비슷한 자유에너지를 가진 다른 형태를 가져서는 안 된다. - 즉, 자유에너지 최솟값이 유일해야 한다 (경쟁자가 없어야 함).
-
- 안정성 (Stability) - 주변 환경의 작은 변화가 최소 에너지 형태의 변화를 일으켜서는 안 된다. - ==자유에너지 표면이 접시(여러 개의 비슷한 낮은 에너지 상태들이 있는)가 아니라 깔때기(native state가 바닥에 있는) 모양이어야 한다.== - Native state 주변의 자유에너지 표면이 충분히 가파르고 높아야 안정성을 제공할 수 있다. → 살짝 모양이 바뀌어도 다시 native state로 돌아오도록
-
- 운동학적 접근성 (Kinetical accessibility) - 펼쳐진 상태에서 접힌 상태로 가는 자유에너지 표면의 경로가 합리적으로 부드러워야 한다. - 다시 말해, 사슬의 폴딩 과정이 매우 복잡한 형태 변화(매듭이나 다른 고차 형태)를 포함해서는 안 된다. - 단백질 형태의 기본적인 변화는 환경에 따라 일어나며, 그 자리에 맞게 형태를 바꾼다. - 이것이 생체분자가 여러 형태로 전환할 수 있는 다중 구조를 만든다.
원래는 모든 경우의 수가 에너지가 동등하다고 가정 → 평평하고 뾰족한 깔떼기 (Levinthal paradox의 상황이다)
실제로는 모든 경우의 수가 에너지가 다름 → 부드러운 깔떼기
differential scanning calorimetry (DSC)
열량 측정장비, 마이크로스케일로.
엔트로피를 측정하고 싶다. 그런데 이게 안되니까, 비열을 측정하자.
온도가 달라질 때 엔탈피가 얼마나 변할까?
경우의 수가 적으면 열용량이 적어진다.
그러므로 unfolding된 단백질이 열용량이 크다.
folding된 단백질은 열용량이 적다.
→ 무조건 이렇게 말하는 게 맞아?
정압 비열 (Constant Pressure)
온도변화에 따른 엔트로피 변화가 커질 수록 비열이 커진다!!
이제보니 비열과 엔트로피가 동차원이구나.
이 장비는 온도를 설정해 두고, 온도 변화에 따른 열 출입을 측정한다. Q(T)를 측정한다는 거다.(실제로는 열 투입에 쓰인 전기 에너지) 같은 온도를 겪는 샘플과 열 출입량을 비교한다.
뭘 측정할 수 있는가?
- 상전이 측정 (녹는 점, 지질구조물)
- 단백질의 접힘과 풀림에 대한 실험
- pH 조건에서 효소의 안정성
- 독립적인 도메인의 수를 유추할 수 있다. (melting temperature가 몇 번이나 있는지 확인하여서)
- 작은 리간드가 붙고 떨어지는 열용량 차이 (리간드 자체의 열용량이 없어야 함) 리간드가 붙으면 folding릐 효과가 나면서 열용량이 적어져야 한다. 그리고 T_m이 늘어나야 한다. 안정적이니까.
레퍼런스가 꼭 필요하다.
레퍼런스와 샘플의 온도 상승 지연을 만회하기 위한 추가 열을 측정한다.
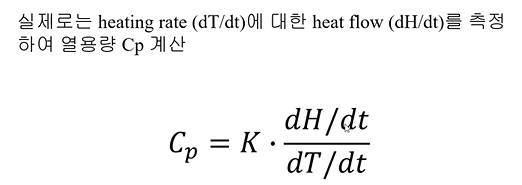
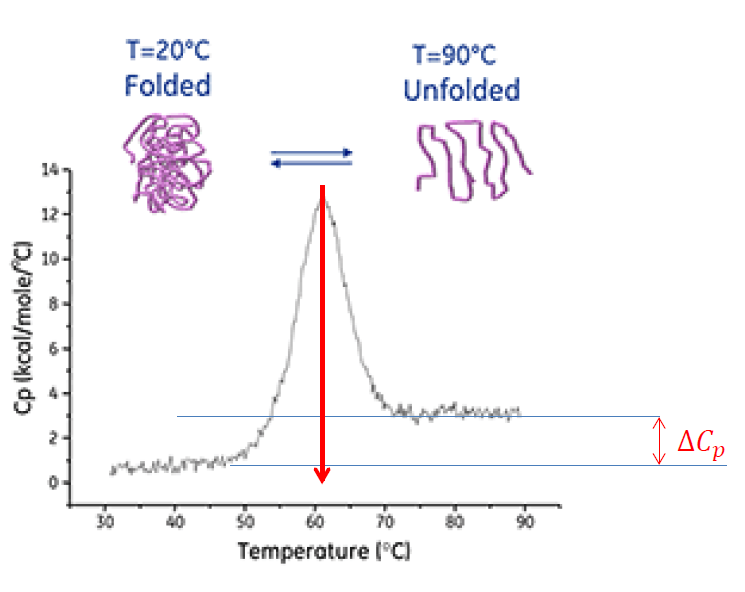
상전이에서는 비열이 무한대로 뛰는 경향
오른쪽으로, 풀림 이후에는 열용량이 높아졌다. 이런 방식으로 melting temperature(
이렇게 두가지 상태의 열용량 차이를 알 수 있다.
열용량을 온도로 적분하면 엔탈피가 나온다.
저 그래프 아래를 적분하면 특정 온도에서 다른 온도에 도달하기 까지의 엔탈피 변화를 알 수 있다.
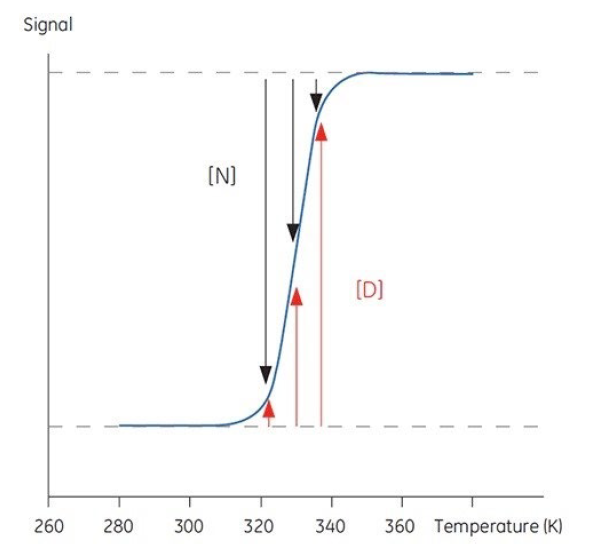
그래프에서 나오는 시그모이드 커브는 비율을 나타낸다. 두 가지 상태의 비율.
시그모이드 커브는 변화량 대비 관찰량을 근사한 그래프로 그릴 수 있다. 이 시그모이드 커브를 이용해 특정 변수(여기서는 온도)에서 평형 상수를 구할 수 있다.
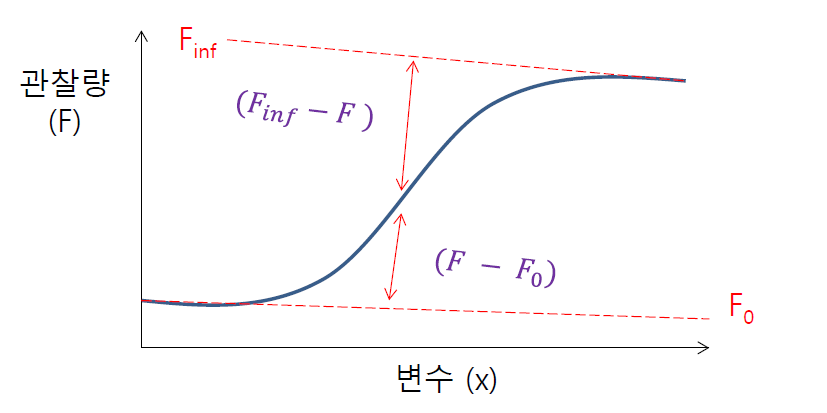
위 이미지에 따르면 특정 x에서 K값은
그러면 T 알고 K아니까 깁스자유에너지 변화도 알 수 있다.
isothermal titration calorimetry (ITC)
단백질 상호작용의 열을관찰하기 위해
두 종류의 단백질을 넣고 열용량의 변화를 동시에 측정.
온도 일정 유지. 반응물을 방울방울 똑똑.
- 친화도 (혹은 해리상수수)
- 결합기작 (엔탈피에 변화를 주나? 엔트로피에 변화를 주나?)
- 결합부위 수 (stoichiometry)
- 동역학적 정보
이제는 분리 상수에 관한 식이다.
두 가지 상태는 분리된 상태와 결합한 상태.
분리 상수 K (dissociation constant)
총 리간드 농도랑 총 리셉터 농도는 알고 있다.
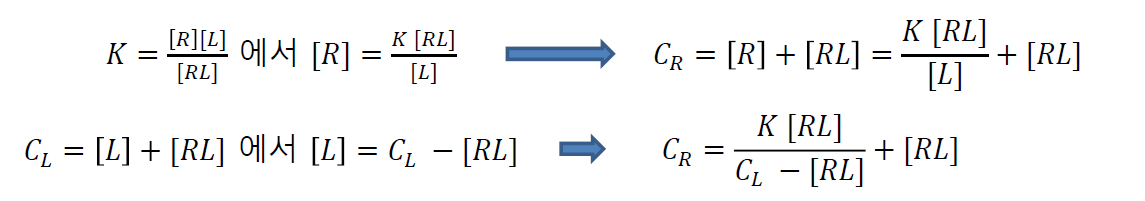

K는 측정을 통해 알 수 있다. 그러면
형광 표지 안 해도 된다.
S, T, H 모두 볼 수 있다.
butter를 많이 타는 게 문제.
이온과 거품에 민감.
시료가 많이 필요한다. 단백질을 열~~ 심히 만들어야 한다.
DSC와 공통점
- 실시간 용액 실험
- 열용량 변화(엔탈피 변화) 측정
- 히터와 온도 센서 사용
- 샘플과 레퍼런스 비교
DSC와 차이점
- 한 분자 VS 두 분자의 결합 상태
- 주사기로 ligand 적정
- stirrer가 있음
- 상태 변화에 따른(리간드 투입에 따른) 온도 변화를 보상하기 위해 투입된 열을 측정
heat pulse → 리간드가 결합할 때 방출되는 에너지
곡선의 중간 slope를 구하면 1/K_d 가 나온다. 왜? 이것이 affinity이므로. 해리 상수와 affinity는 inverse이다.
더불어 엔탈피 변화량도 구했다. (왜인지는 모르겠지만)
그리고 결합수(stoichiometry) n도 구할 수 있다.
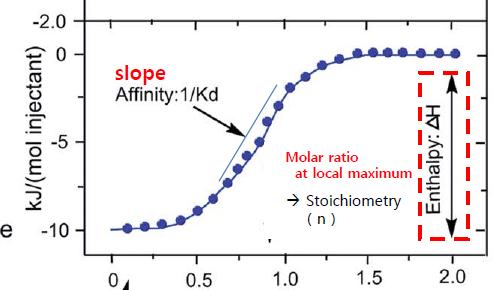
K를 구했으니
S도 구할 수 있다.
Entropy 변화 vs Enthalpy 변화
ITC를 동해 S와 H중 어떤 변화가 우세한지 알 수 있다.
- Entropy가 변화한다? hydrophobic interaction이나 conformational change에 의한 열량 변화가 일어난다.
- Enthalpy가 일어난다? hydrogen bond등으로 에너지 흐름이 있었다. 실질적인, 정전기적인 원자의 반응.
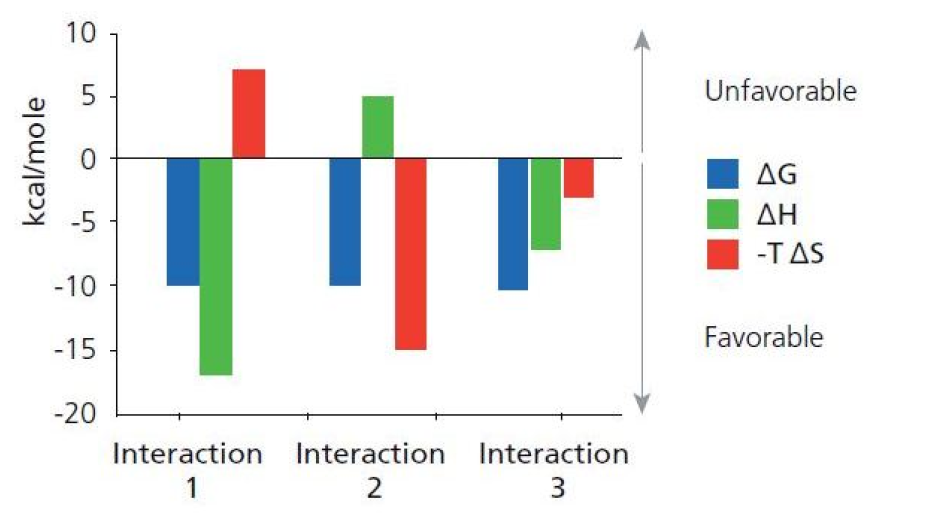
음수값이 큰 parameter가 안정화에 더 많이 기여한다는 뜻. 1번은 엔탈피가 더 큰 기여, 2번은 엔트로피가 더 큰 기여.
microscale thermophoresis (MST)
리간드 affinity를 구하는 방법
형광 표지가 필요하다.
K_d를 측정하긴 하지만 H, T, S를 측정하지는 않는다.
사용이 빠르다. 20분 만에 가능.
적은 시료로도 된다.
열변성에 취약. 데이터를 사용할 수 없다. 단백질이 열 변성에 취약하면 어쩌지?
여러 농도로 리간드를 섞은 capillary 준비!
적외선 레이저로 가열.
열때문에 입자가 밀림. 레이저 부위의 형광 신호가 사라짐
레이저가 꺼지면 다시 형광 신호가 돌아옴.
만약에 리간드가 리셉터에 잘 붙들어져 있어서 운동성이 낮아졌다면? 열에 의해 밀리는 정도가 줄어들기 때문에, 레이저를 쏘아도 형광 신호가 적게 줄어든다.
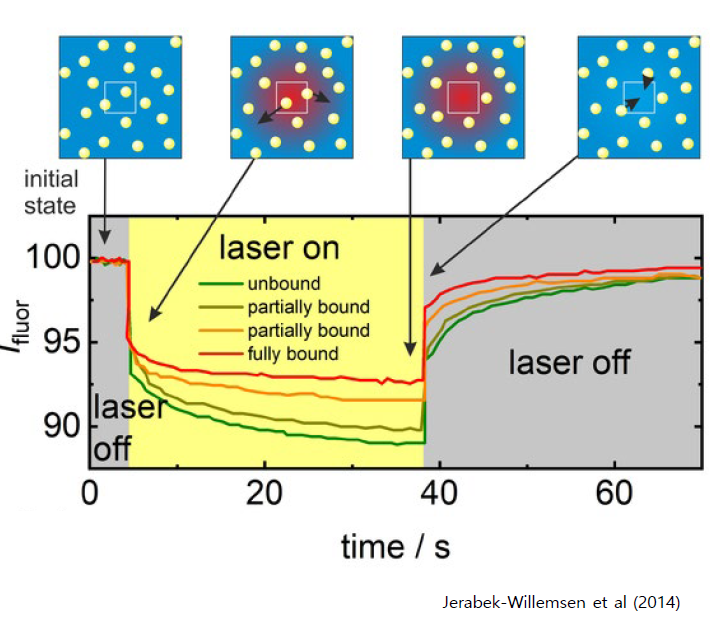
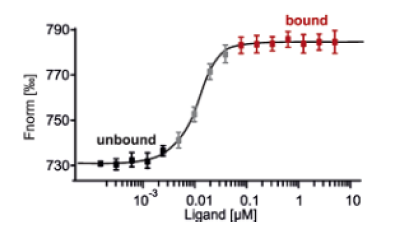
어라? 시그모이드다! 평형 상수를 구할 수 있다.
K_d를 어떻게 구할 수 있었더라???
differential scanning fluorimetry
역시 리간드 affinity를 구하는 방법
리셉터에 리간드가 달려있으면 온도가 높아도 단백질이 잘 안 풀린다.
리간드가 있을 때 없을 때 언폴딩되는 온도 차를 보자.
unfolding 되었는지 어떻게 아냐고요?
unfolding된 단백질에 잘 붙는 형광 다이를 사용.
형광이 많이 나타나면 unfolding 완성.
트립토판이나 타이로신이 가진 자체 단백질 형광을 볼 수도 있다.
마이크로몰 수준의 친화도는 잘 보지만 그 보다 적은 건 좀…
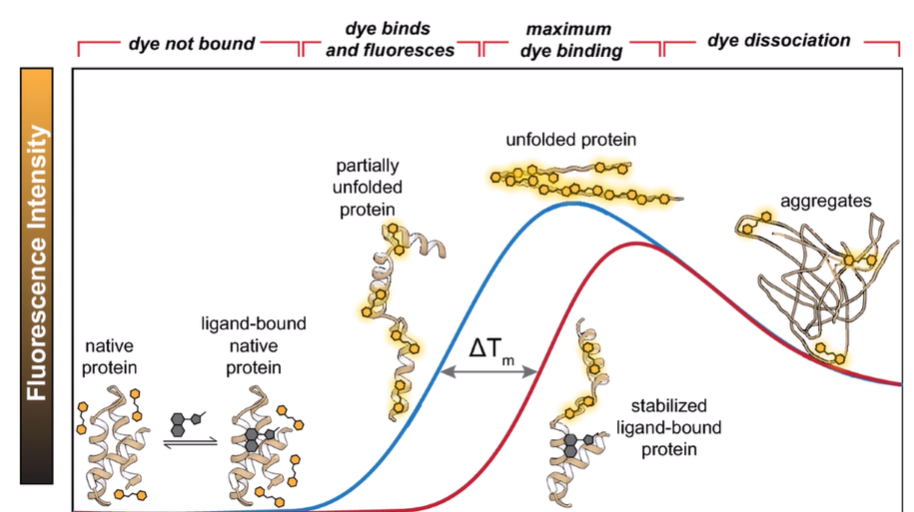
리간드가 붙으면 T_m이 높아진다.
높은 온도에서 버틸 수 있게 튼튼
이러면 리간드 농도에 따른 Tm 그래프를 그릴 수 있고, 이를 통해 다시 K_d 값을 구할 수 있다.
한계! 아쉬운 점
Dye가 문제야. Dye와 리간드가 상호작용하면 어쩔건데?
nM 단위에서는 못 함. 마이크로몰 정도는 되어야 함.
equilibrium dialysis
리간드가 통과할 수 있는 반투막.
한쪽 공간은 리셉터가 있고, 다른 공간은 없다.
양쪽의 농도 차이를 이용해 affinity를 구할 수 있다.
전제는? 양쪽의 자유 리간드 농도가 같다고 가정.
양쪽에서 절대적 리간드 농도 차는 곧
이제 K값 구할 수 있겠죠?
한계!
리간드가 반투막보다 크기가 크면 그냥 못 하는 실험.
UV 흡광도에 따른 농도를 알 수 있는 흔한 리간드라면 제일 좋은 실험.
surface plasmon resonance(SPR) (중요)
광학장비면서 세척장비다?
리간드와 붙은 리셉터를 계속 씻어서 리간드가 얼마나 잘 떨어져 나가는지 확인한다.
아주 얇은 박막에서 일어나는 간섭현상.
금 박막에 단백질을 붙인다.
전반사 일으켜서 evanescent wave가 얼마나 흡광되는지 본다.
즉 반사가 얼마나 잘 되는지 본다.
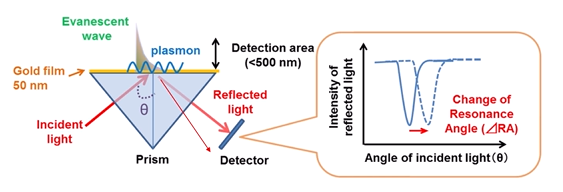
단백질이 붙어있으면 반사광의 peak의 각도가 달라진다. resonance angle의 차이가 생김.
리간드가 붙어 있어도 peak 위치가 달라짐.
아주 미량의, 그리고 아주 작은 affinity도 감지할 수 있다.
기계가 자동적으로 돌아가서 좋다.
그런데 기계 비싸다.
장비를 재활용하느라 더러워진다.
biolayer interferometry(BLI)
원리는 위와 똑같다.
입사각 대신 파장을 바꾼자.
그런데 더 비싸다.
quartz crystal microbalance (QCM)
석영은 압력을 주면 전기 생김.
질량 차이를 알 수 있다. 적룔 전류와 진동수를 기록해서.
정성적인 측정법
SDS page
gel filteration
Co-IP → 일단 붙는지 아닌지는 알 수 있음.
Forster resonance energy transfer (FRET)
알지!! 표지를 하면 일단 정량 측정을 할 수 있어.
함께 생각해 볼까요?
열로 볼 수 있는 분자의 상태 변화는 또 뭐가 있있을까>
물리 화학적 성질을 이용하여 새로운 측정 장비를 만들 수 있을까
적어두 두세개의 장비로 측정해야 논문으로 쓸 수 있다.
2차 시험 이창훈 교수님 전기 강의
갈바니 전기
볼타 전지
생명현상에서 전기를 볼 수 있는 곳은?
전기뱀장어 사냥
전기뱀장어와 아주 큰 사냥꾼 사이에 전류는 어떻게 흐르는 거지?
물을 경유해서 회로를 만든다.
논문 저자 이름 누구였어요???
전기뱀장어의 Hunter’s organ
electrocyte
mV 차이가 어떻게 감전까지 일으키지? 겹겹이라서?
사람도 전기 쓴다. 심장에
SA node
electromyogram(EMG)
근육의 수축도 근육으로 측정해보자.
trans-epithelial electrical resistance (TEER)
조직이 건강하면 조직을 통과하는 전류에 대해 저항이 강할 것이다.
세포 조직은 capacitance도 있다. 이걸 측정할 수도?
교류를 이용한다. 이걸로 다른 정보를 알 수도?
수식은 안 외워도 돼요!
TEER은 바이오칩에서 조직이 잘 만들어졌는지 확인하는 용도로도 사용한다.
action potential
Electro Encephalo Graphy (EEG)
여러 개의 신경세포에서 나오는 전기장을 함꺼번에 측정
뉴련 단위가 아니라 뇌 단위의 단서 제공.
MAOA 유전자에 따라서 EEG 신호가 달라졌다고 한다.
magneto encephalo graphy
전류에서 유도된 뇌의 자기장도 측정가능할까? 물론!
장비가 정말 크다!! EEG보다 해상도가 좋다고 한다.
센서는 작은데 왜 장비 크기는 클까.
아주 작은 전기장을 잡아야 해서 초전도 수준으로 온도를 낮춰야한다.
superconducting quantum interference device
지구 자기장으로 인한 노이즈는 어떡하지?
지구자기장을 차폐해야 뇌의 아주 미약한 뇌의 자기장을 잡을 수 있다.
지자기를 사용하는 미생물
magnetosprillum magnectotactium
몸 안에 나침반이 있는 미생물.
철을 먹어서 몸 안에 자석을 만든다.
어떻게 원자단위로 자성을 정렬하죠? → 물리학자들이 보면 까무러칠 거 같은데?
같은 종이어도 남반구에 있는 애랑 북반구에 있는 애랑 행동이 거울상이래요.
내가 땅속 적당한 깊이에 있는지 나침반으로 확인한다고 한다?
electron을 호흡하는 박테리아?
SDS page
Clarity 기법
세포가 불투명한 이유는 지질때문()이게 산란 일으킴
세포 전체를 하이드로젤로 고정시키고, 지질만 씻어 없애버린다.
이때 SDS page를 이용해 지질을 제거한다.
iontophoresis
약이나 화장품을 피부에 효과적으로 전달하고 싶을 때
electro spray ionization MS
실험에서 전기장을 쓰고 싶다면
시료는 전하를 띄어야 한다.
Buffer 전해질이 필요하다.
전기장의 크기는 분자의 성질과 매질의 성질에 따라 결정.
이건 꼭 알아라!!!
전하에 의해 받는 전기력과 마찰력이 평형을 이룸.
이때 속도를 이용해서, 그리고 마찰계수에 의해, 전하량에 의해, 입자의 크기를 알 수 있다.
다만 매질의 점성을 잘 알아야 한다.
DLS같은 걸로 확산 계수를 측정한다면 좋겠네?
SDS만 이용하면 적어도 크기의 상대값을 알 수 있다.
electrophoretic mibility
d는 이동 거리
U에 로그를 씌우면 선형적이다.
유교수님 2차 시험
통계 역학
바이오에서 가장 많이 쓰임
생명에는 입자가 많으니까.
슈뢰더 thermal physics
라이프 Fundamentals of thermal and thermal physics
패트리아
따로 정리한 학습 노트들
전부다 템플릿에 맞춰 수정해야 함
microcanonical ensemble의 entropy
여러 시스템의 미시 상태 수 예제
이상 기체의 미시 상태 수
canonical ensemble에서 Boltzman factor
partiton function in canonical ensemble
프로틴 시뮬레이션과 몬테카를로 시뮬레이션
메트로폴리스랑 detailed balance를 잘 알아야 하지요호!
왜 컴퓨터 시뮬레이션으로 연구해야하는가?
실험으로 찍지 못 하는 구조가 있기 때문. 실시간 움직임을 볼 수 없다.
반도체는 시뮬레이션하면 실험하고 90%일치한다.
단백질은? 20%이다.
왜 바이오는 실험과 일치하는 시뮬레이션을 만드는게 힘든가.
몬테카를로 시뮬레이션: 컴퓨터에게 시키는 확률적 반복 작업
몬테카를로가 뭘까. 그냥 확률 시행을 일일이 진행하는 게 몬테카를로다. 확률 시행을 여러번 하여 결과가 어떻게 나오는지 한번 보자.
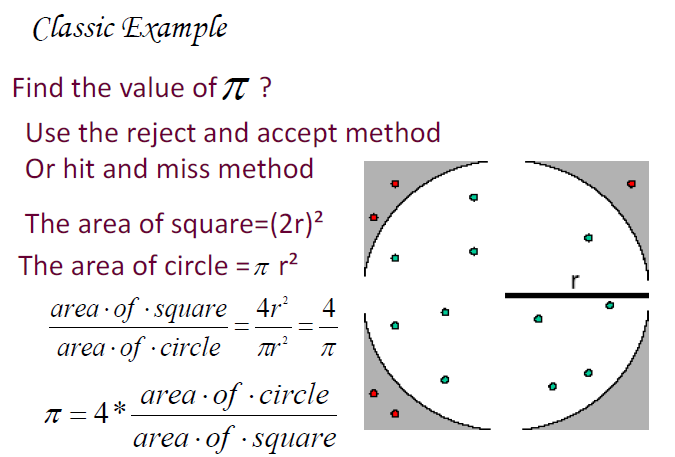
고전적인 예시) 원판에 다트 던져서 원주율 알아내기
적분 못 하는 값도 구하는 몬테카를로
랜덤 위치에 점을 던져서 적분하고자 하는 영역 안에 있는지 비율을 알아내면 끝이라고!
Markov state model
Markov Property → 아직 노트 안 만들었다
나에게 과거는 없어.
오로지 현재 상태를 통해 다음 어떤 상태로 갈지가 결정.
지금 상태가 A일 때, 다음으로 B로 전활될 확률이 정해진 시스템.
이 확률들을 matrix 형태로 적을 수 있겠지?
Markov State Model
Markov Property를 따르는 시스템.
나에게 과거는 없어. 오로지 현재 상태를 통해 다음 어떤 상태로 갈지가 결정된다.
지금 상태가 A일 때, 다음으로 B로 전환될 확률이 정해진 시스템.
이 확률들을 matrix 형태로 적을 수 있다.
Transition Probability Matrix
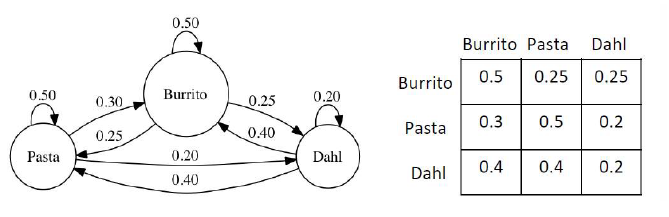


만약 상태를 행벡터로 나타낸다면 (i번째 요소는 현재 i번째 상태에 있을 확률):
-
transition probability matrix에서
-
m번째 행은 ‘현재’ 상태가 무엇인지
-
n번째 열은 ‘다음’ 상태가 무엇인지를 나타낸다
-
즉
은 m이라는 현재 상태에서 n이라는 미래 상태로 전환될 확률을 나타낸다. -
따라서 transition probability matrix의 각 행의 합이 모두 1이다. (현재 상태 m에서 출발하면, 어딘가로는 반드시 가야 하므로) 상태 벡터를
(행벡터)라고 하면: 이렇게 곱해서 다음 시간의 상태 분포를 얻는다.
Detailed balance를 따르는 transition probability에는 뭐가 있지?
Glauber dynamics
이름 안 외워진다. Glauber!! Glauber!!!
두 상태의 전환이 일어날 확률은
그러니까, 현상태 A이고 이동할까 말까 고민하는 후보 상태가 B라면,
둘의 Boltzman factor 중 B가 우세한 비율을 계산한다.
응! 지금 상태 말고! 변화할 상태가 우세한 정도를 보는 거다.
B의 Boltzman factor를 A와 B의 Boltzman factor의 합으로 나눈다.
이게 왜 detailed balance를 따르는지는 금방 알 수 있다.
Matropolis dynamics
에너지가 높은 상태에서 낮은 상태로 전환할 확률은 1이다. (에너지가 낮아지는 경우는 묻고따지지도 않고 그냥 전환)
에너지가 낮은 상태에서 높은 에너지로 전환할 확률은
즉 정리하면,
에너지가 낮→높으로 가는 건
이렇게 시뮬레이션하다보면 볼츠만 분포에 따라 평형상태가 된다.
왜냐고?
-
인 경우, , -
그 반대인 경우
에서 증명해봐라. 간단하다!
단백질 시뮬레이션하기
단백질 분자속 원자만 2천개.물분자 2만개. 어떻게 시뮬레이션해.
물 없애자! 곁사슬 없애자! 아미노산산을 하나의 비드로 보자! 3차원 말고 격자를 쓰자!
몬테카를로 시뮬레이션 (메트로폴리스…0…)
잔기를 랜덤하게 하나 고른다. 플립하면 어떤 에너지가 될지 계산한다. 에너지에 따라 플립할지 말지 결정한다.

가장 간단하게는 single residue를 two-state system으로 보는 것이다.
flip할 것인가, 말 것인가, 둘 중 하나로. 이걸 몬테카를로로 업데이트해 간다.
lattice model
신기하다.
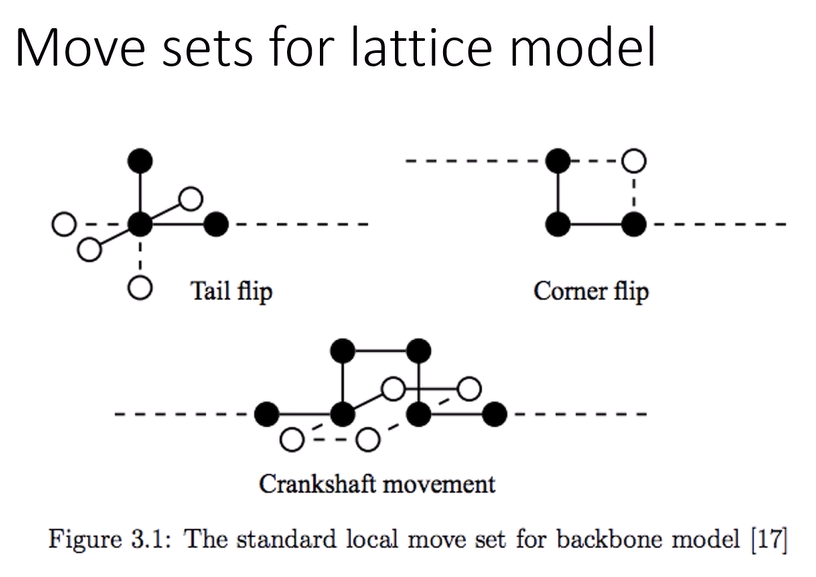
세 가지 전환 방법이 있다.
Molecular dynamics simulation
전기
물리과에서 배우는 전자기학(미분방정식의 특수함수)과 생명에서 쓰는 전자기학의 간극.
생명에서는 회로를 더 많이 쓴다.
내가 지금 계산 뇌 강의에 왔나요?
gene regulation도 서킷인가?
전사량과 단백질 발현 양의 상관관계는 그리 높지 않다. (70% 정도)
측정 장비에서 전자기역학?
RC, LC, RCL 회로
빵판.
V= IR
Q = CV (이게 C의 정의다.)
V = L dI/dt 인덕턴스틑 전루 변화량에 의해 전압을 유도한다. 솔레노이드 전자기 유도. 전류의 급격한 변화를 막는다.

저항과 캐퍼시터의 합성
RC 회로
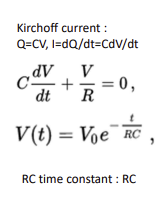
캐페시터의 충전 전하의 시간 변화가 곧 전류이다,
미방을 풀면 전압이 지수적으로 변화한다는 것을 알 수 있다.
LR 회로
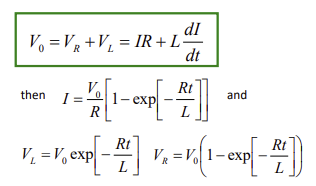
LC 회로
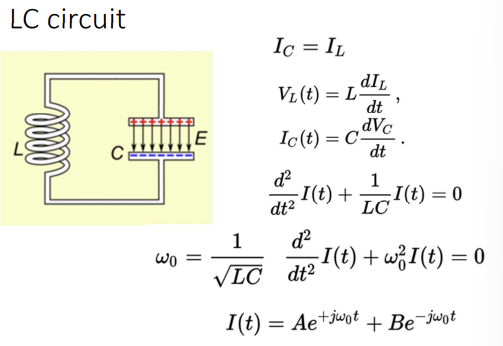
RLC 회로
damped harmonic oscillator
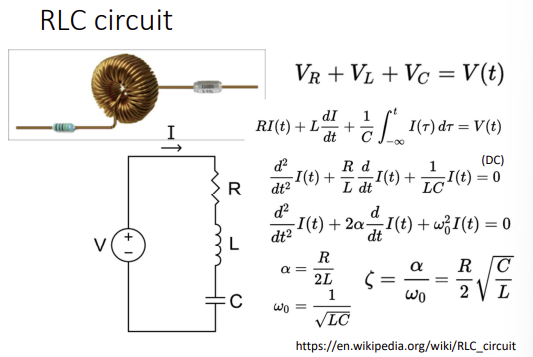
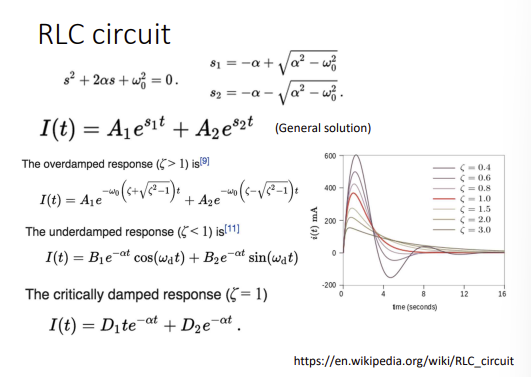
RLC 회로를 언제 쓰는가?
주파수 성분을 거르고 증폭하기 위함. 공명진동수
키르히호프 규칙
한 점에서 전류 in out은 0
한번 회전하면 전압이 0
맥스웰 방정식 → 파방
진공(전하 없음) 상태에서 맥방 풀면 파방 나온다 → 이 과정 외우기?
nerve conduction
오히려 랑비에 결정에서 신호가 증폭된다?
나트륨 펌프가 있기 때문
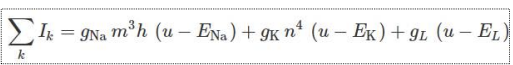
data fitting이 운 좋게 잘 된 예
n h m
n은 K꺼,
m과 가 나트륨꺼.
g는 conductivity
u는 막전위
채널이 딱 4개 영역으로 이루어졌기에 망정이지.
각 term의 의미가 뭔가?
m은 Na channel 활성화 게이트, h는 Na channel 비활성화 게이트, 닫히게 만든다.
n은 K channel 활성화 게이트
회로도 그리기.
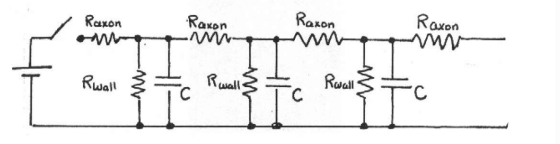
HH model
이온 채널 개패를 가변 저항으로.
회로 그림이랑 각 parameter 의미 알아두기
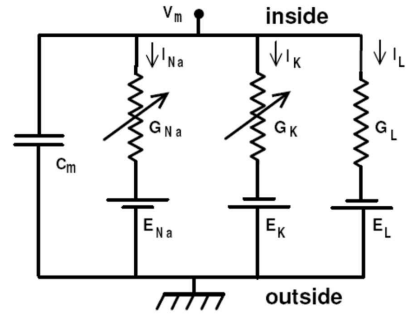
평형 전위 음수 양수 중요?